В настоящее время кардиотоксичности, развивающейся на фоне проведения противоопухолевого лечения, уделяется большое внимание. Это связано с тем, что в современной онкологии используются новые, более интенсифицированные схемы лечения, что, в свою очередь, увеличивает риск развития побочных эффектов, в том числе и со стороны сердечно-сосудистой системы. В статье описаны кардиологические осложнения, связанные с химиотерапией опухолей, лучевые поражения сердца составляют отдельную тему.
Использование новых схем химиотерапевтического лечения ведет к удлинению срока безрецидивной выживаемости и увеличению числа пациентов, излеченных от онкологических заболеваний. Следует указать, что среди этих больных большую часть составляют работоспособные пациенты, а развитие кардиологических осложнений на фоне химиотерапии ведет к ухудшению качества жизни и снижению ее продолжительности у потенциально излечиваемых пациентов, особенно уже имеющих сердечно-сосудистые заболевания.
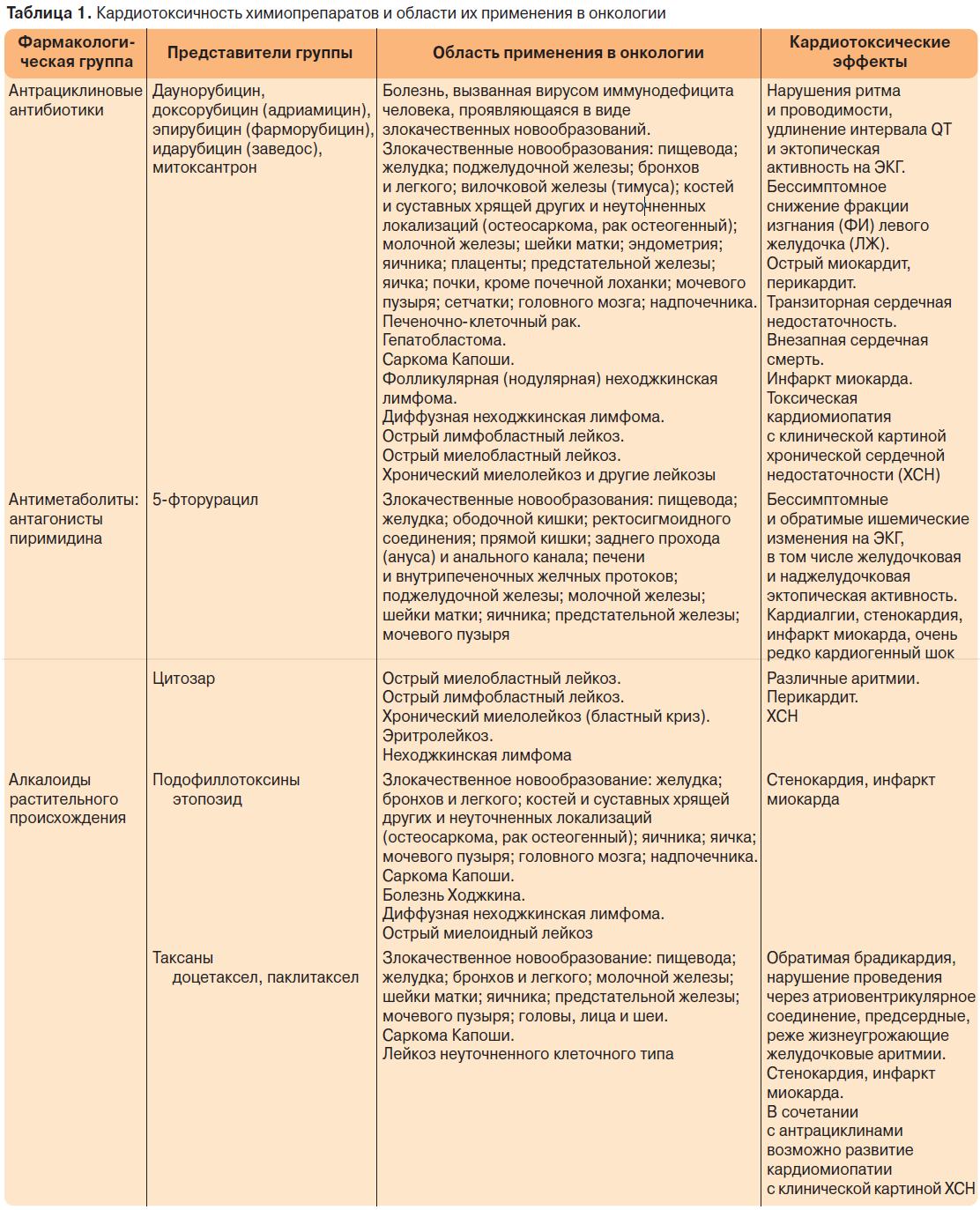
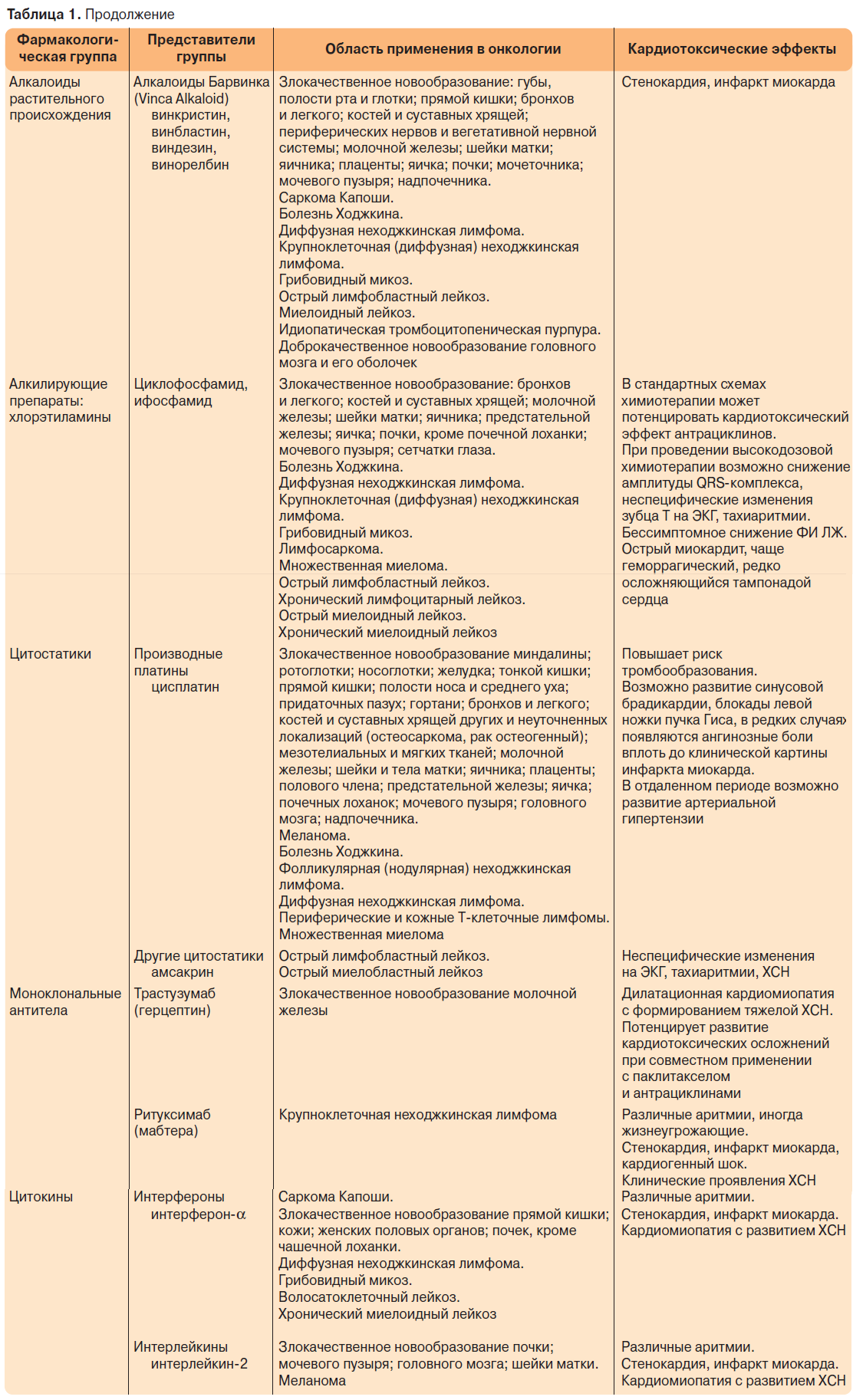
Многие химиотерапевтические препараты обладают кардиотоксичностью, однако в настоящее время описано большое количество случаев кардиологических осложнений, развивающихся на фоне введения антрациклиновых антибиотиков, что связано с их высокой противоопухолевой активностью, а также с широким их применением в различных схемах химиотерапевтического лечения. Антрациклиновые антибиотики используются преимущественно в составе различных схем химиотерапии, поэтому об “антрациклиновой кардиотоксичности” при появлении кардиологических осложнений можно говорить условно. Помимо антрациклиновой описана кардиотоксичность и многих других химиотерапевтических препаратов, ниже представлены препараты, на фоне введения которых могут развиваться кардиологические осложнения (табл. 1).
В настоящее время определены факторы риска развития кардиологических осложнений при применении противоопухолевых препаратов, к которым относятся: суммарная доза препарата (характерно в большей степени для антрациклинов, например, для доксорубицина кумулятивная доза составляет 500–550 мг/м2); общая доза, введенная за день или за курс химиотерапии; скорость и порядок введения препаратов; облучение средостения в анамнезе; возраст (младше 15 и старше 65 лет); женский пол; одновременное введение других противоопухолевых средств (циклофосфан, блеомицин, этопозид, цисплатин, винкристин, актиномицин, метотрексат); предшествующая терапия антрациклиновыми антибиотиками; сопутствующие заболевания сердечно-сосудистой системы; дисбаланс электролитов (гипокалиемия, гипомагниемия).
На данный момент нет единой классификации кардиотоксичности химиотерапевтических препаратов, которая может развиться в различные сроки от начала лечения. Для антрациклиновых антибиотиков принято разделение кардиотоксичности по срокам ее возникновения на острую, подострую, хроническую и позднюю хроническую.
Острая антрациклиновая кардиотоксичность развивается в момент введения или в течение 24–48 ч после введения препарата и, по сообщениям разных авторов, наблюдается в 0,4–41,0% от общего числа случаев антрациклиновой кардиотоксичности. Она проявляется бессимптомным нарушением реполяризации на ЭКГ, снижением вольтажа QRS-комплекса, развитием синусовой тахикардии, появлением желудочковой и наджелудочковой экстрасистолии, увеличением интервала QT. Возможно также бессимптомное снижение фракции изгнания (ФИ) левого желудочка (ЛЖ). Известны случаи развития острого миокардита или миоперикардита, транзиторной сердечной недостаточности на фоне введения антрациклинов. Исключительно редко наблюдались случаи внезапной смерти и инфаркта миокарда. Описанные изменения на ЭКГ считаются обратимыми, часто протекают бессимптомно и регрессируют в течение 1 мес после окончания химиотерапии. Однако у этой группы больных имеется опасность развития хронической сердечной недостаточности (ХСН) в отдаленные сроки после окончания лечения основного заболевания.
Подострая кардиотоксичность встречается редко, в основном она проявляется токсическим перикардитом и/или миокардитом спустя несколько недель после последнего введения антрациклиновых антибиотиков.
Для хронической и поздней хронической кардиотоксичности характерно развитие кардиомиопатии с клинической картиной ХСН в течение 1-го года или спустя десятилетия после окончания противоопухолевого лечения соответственно. По данным литературы, кардиомиопатия, развивающаяся на фоне лечения антрациклиновыми антибиотиками, может быть как дилатационной, так и рестриктивной, что не всегда определяется дозой препарата. По нашим данным, у 27,6% больных, которые получают комбинированное лечение, включающее антрациклины, в отдаленном периоде после окончания химиотерапии возможно развитие так называемой неклассифицируемой кардиомиопатии, которая проявляется снижением ФИ ЛЖ без дилатации его полости при постепенном увеличении конечного систолического объема (КСО) ЛЖ. А во время проведения химиотерапевтического лечения происходит статистически значимое снижение конечного диастолического объема (КДО) и его индексированного значения. В дальнейшем, в течение 6 мес после завершения химиотерапии у пациентов с ХСН, развившейся после лечения антрациклинами, КДО ЛЖ продолжает снижаться, а у больных без ХСН возвращается к исходному уровню.
Пациентов чаще всего беспокоит снижение переносимости физической нагрузки и одышка различной степени выраженности, что иногда принимается врачом за проявления основного заболевания и остается недооцененным. Согласно принятым рекомендациям, больные с развившейся симптоматикой должны получать стандартную терапию ХСН. Однако, по мнению разных авторов, на фоне кардиотропной терапии дисфункция ЛЖ не всегда полностью обратима. Фармакологическое лечение может улучшить качество жизни и снизить количество осложнений, однако для антрациклиновой кардиомиопатии характерен плохой ответ на лечение и соответствующий плохой прогноз, смертность составляет 27–61%. При развитии кардиологических осложнений в течение первых 4 нед после окончания химиотерапии прогноз наиболее неблагоприятен.
Поздняя хроническая кардиотоксичность протекает субклинически и носит прогрессирующий характер, часто она развивается у пациентов, которые получили относительно низкие дозы антрациклинов – менее 480 мг/м2. Следует отметить, что длительное бессимптомное течение кардиотоксичности особенно характерно для детей. При использовании паклитаксела кардиотоксичность развивается у 30–35% больных, она проявляется обратимой брадикардией на ЭКГ; в 0,5% случаев возникают предсердные, реже жизнеугрожающие желудочковые аритмии, нарушения проводимости; еще реже возможно развитие ишемии или инфаркта миокарда. Паклитаксел потенцирует кардиотоксический эффект антрациклиновых антибиотиков за счет снижения почечной экскреции, что ведет к увеличению времени циркуляции антрациклинов в плазме.
Для 5-фторурацила характерно развитие ишемии миокарда за счет спазма коронарных артерий, что встречается в 3–8% случаев. Характерными симптомами являются кардиалгии, предсердные и желудочковые аритмии, довольно редко развивается инфаркт миокарда и кардиогенный шок. В 60–65% случаев от общего количества кардиологических осложнений на фоне введения 5-фторурацила проявления ишемии миокарда ограничиваются бессимптомными изменениями на ЭКГ, при этом уровень кардиоспецифических ферментов не повышается. В большинстве случаев кардиотоксичность 5-фторурацила проходит после его отмены или на фоне лечения антиангинальными препаратами.
Кардиотоксический эффект трастузумаба проявляется бессимптомным снижением ФИ ЛЖ, что в дальнейшем ведет к развитию дилатационной кардиомиопатии. При использовании трастузумаба в качестве монотерапии она развивается у 4–8% пациентов, среди них явления тяжелой сердечной недостаточности (III–IV функционального класса по NYHA) встречаются у 0,6–4,1% больных. При применении трастузумаба в комбинации с другими противоопухолевыми препаратами, такими как антрациклины и паклитаксел, кардиотоксический эффект увеличивается. Важно то, что кардиологические осложнения на фоне использования комбинации трастузумаба с паклитакселом обратимы, а при комбинации с антрациклинами – нет. Трастузумаб наряду с ритуксимабом и бевацизумабом входит в группу моноклональных антител, используемых в таргетной терапии онкологических заболеваний, их эффект опосредуется ингибированием тирозинкиназ, которые играют ключевую роль в передаче клеточного сигнала. Ко второму классу таргетных препаратов относят малые молекулы ингибиторов тирозинкиназы (лапатиниб, иматиниб, сорафениб, сунитиниб), которые широко используются в лечении метастатического рака почки, рака молочной железы, толстой кишки, легкого, желудочно-кишечных стромальных опухолей и хронического миелолейкоза. Кардиотоксичность, развивающаяся на фоне применения ингибиторов тирозинкиназы, может проявляться снижением ФИ ЛЖ с последующей клинической картиной ХСН, нарушениями проводимости, в том числе с удлинением интервала QT на ЭКГ, острым коронарным синдромом и артериальной гипертензией. Механизмы развития кардиотоксичности ингибиторов тирозинкиназы в настоящее время изучаются как онкологами, так и кардиологами.
Алкилирующие агенты, в частности циклофосфамид, в стандартных схемах химиотерапии способны лишь потенцировать кардиотоксический эффект антрациклинов. А при проведении высокодозовой химиотерапии кардиотоксичность циклофосфамида проявляется снижением амплитуды QRS-комплекса, неспецифическими изменениями зубца Т на ЭКГ, тахиаритмиями, бессимптомным транзиторным снижением ФИ ЛЖ. Также возможно развитие острой или подострой, как правило обратимой, сердечной недостаточности. Наиболее часто у таких пациентов возникает острый миокардит, возможно развитие геморрагического миокардита, в редких случаях осложняющегося тампонадой сердца.
Для цисплатина характерно увеличение риска тромбообразования, что в очень редких случаях проявляется ангинозными болями, вплоть до развития инфаркта миокарда, а в отдаленном периоде – артериальной гипертензией. Чаще всего кардиотоксичность цисплатина проявляется синусовой брадикардией, блокадой левой ножки пучка Гиса на ЭКГ.
В 3–4% случаев во время введения митоксантрона или в течение 1-го года после терапии этим препаратом развивается миокардит, токсическая кардиомиопатия со снижением ФИ ЛЖ, также возможно появление аритмии различных типов. В редких случаях при использовании этопозида и винкристина возможно развитие ишемии, вплоть до инфаркта миокарда, что, вероятнее всего, связано со спазмом коронарных артерий.
Под нашим наблюдением находятся пациенты с кардиотоксическими осложнениями, возникшими в различные сроки от начала комбинированного лечения, включающего антрациклиновые антибиотики. Приводим описание двух клинических случаев типичной острой и поздней хронической кардиотоксичности.
Клинический пример 1. Больной О., 27 лет, с диагнозом: лимфома Ходжкина, нодулярный склероз II типа с выраженной эозинофильной инфильтрацией, с массивным поражением медиастинальных и шейных лимфатических узлов, с распространением на мягкие ткани грудной стенки, перикард, левую долю щитовидной железы, стадия IVА. По данным эхокардиографии (ЭхоКГ), проведенной до начала лечения, патологии сердца не выявлено, перед передней стенкой правого желудочка визуализировалось
объемное образование неоднородной структуры.
Химиотерапия у этого больного проводилась по новой схеме ЕА(50)COPP-14 в рамках российского протокола ЛХМосква-1-3. Доза доксорубицина на курс, рассчитанная по поверхности тела, составила 100 мг, что несколько больше дозы, используемой в ранее применявшихся протоколах. Следует обратить внимание на то, что в схему кроме антрациклинов входили препараты, также обладающие кардиотоксическим эффектом, такие как этопозид, винкристин, циклофосфан, в общепринятых дозах.
В первый день химиотерапии проводилось суточное мониторирование ЭКГ по Холтеру, зафиксирована синусовая тахикардия с максимальной частотой сердечных сокращений (ЧСС) 139 в 1 мин; значимой диспозиции сегмента ST, эктопической активности выявлено не было. После первого курса химиотерапии был достигнут значительный противоопухолевый эффект, по данным компьютерной томографии грудной клетки отмечалось уменьшение тени средостения с 11 до 9 см на уровне III ребер.
На 2-й день после окончания полихимиотерапии у пациента появились сжимающие боли за грудиной с иррадиацией в обе руки, слабость. На ЭКГ выявлены инфарктоподобные изменения (рис. 1). В биохимическом анализе крови наблюдалось повышение уровней кардиоспецифических ферментов: креатининфосфокиназы-МБ с 40 до 80 нг/мл, тропонина с 1,3 до 11 нг/мл. Пациент был госпитализирован в отделение реанимации и интенсивной терапии Российского онкологического научного центра им. Н.Н. Блохина РАМН, на фоне введения наркотических анальгетиков ангинозные боли были полностью купированы, в дальнейшем проводилось лечение гепарином, изоптином, кардикетом.
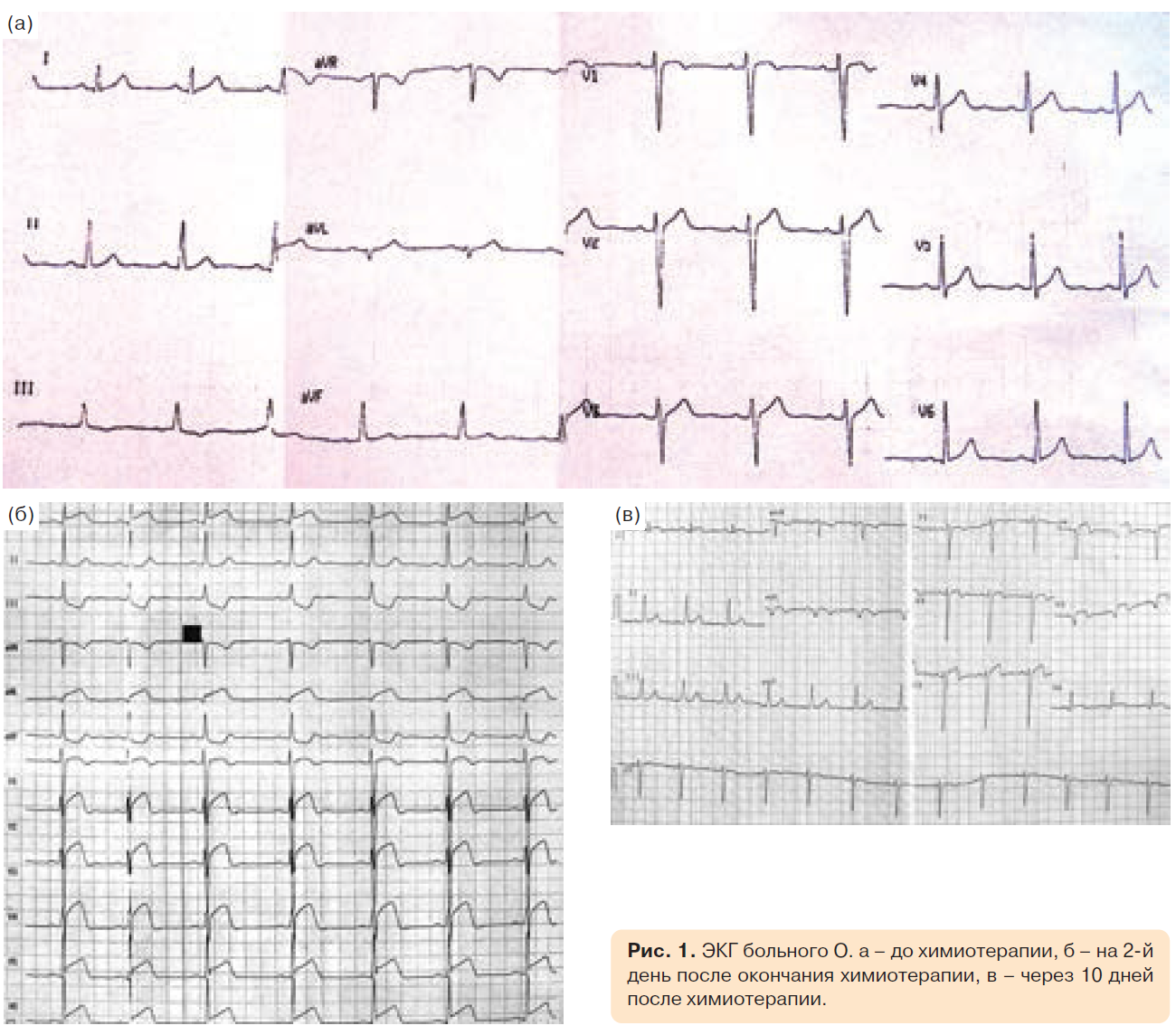
Больной был переведен в городскую клиническую больницу (ГКБ) № 12 (база кафедры госпитальной терапии № 2 Российского национального исследовательского медицинского университета им. Н.И. Пирогова) для дальнейшего наблюдения и лечения. За время нахождения в стационаре проводилась терапия антикоагулянтами, нитратами, титрование доз β-адреноблокаторов (БАБ), ингибиторов ангиотензинпревращающего фермента (ИАПФ), на этом фоне ангинозные боли не рецидивировали, на ЭКГ отмечалась динамика, характерная для переднего инфаркта миокарда (см. рис. 1).
На фоне проводимой терапии уровень кардиоспецифических ферментов снизился, и на 5-й день госпитализации уровни креатининфосфокиназы, тропонинов вернулись к нормальным значениям. При повторном суточном мониторировании ЭКГ по Холтеру также не было выявлено эктопической активности и смещения сегмента ST, однако в вечерние часы сохранялась синусовая тахикардия с максимальной ЧСС до 124 в 1 мин.

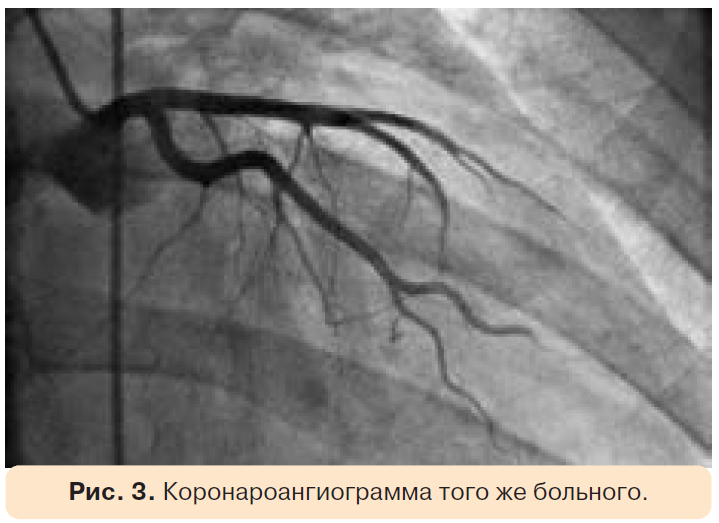
При динамической ЭхоКГ было обнаружено снижение ФИ ЛЖ с 66 до 56,1%, гипокинез верхушечной области и боковой стенки, увеличение КСО ЛЖ с 41,9 до 52,9 мл (рис. 2). Была выполнена коронароангиография. Стенозирования просвета коронарных артерий не отмечено, при этом определялось умеренное замедление скорости смыва контрастного вещества (до 6 сердечных циклов), которое, скорее всего, было обусловлено поражением мелких коронарных артерий, развившимся под воздействием химиотерапевтических препаратов (рис. 3).
Перед выпиской, на 17-й день после окончания химиотерапии проведена контрольная ЭхоКГ, по данным которой показатели систолической функции ЛЖ вернулись к исходным значениям (табл. 2). При этом отмечено уменьшение полости ЛЖ после химиотерапии с последующей его дилатацией, что характерно именно для антрациклиновой кардиомиопатии.
Через 1,5 мес после эпизода острой кардиотоксичности был проведен тредмил-тест. Толерантность к физической нагрузке оказалась высокой, реакция сердечно-сосудистой системы на нагрузку адекватная, тест на коронарную недостаточность отрицательный.
Таблица 2. Динамика показателей ЭхоКГ до и после химиотерапии и на фоне кардиотропной терапии
| Показатель | Перед химиотерапией | После окончания химиотерапии | |
| через 6 дней | через 17 дней | ||
| КДР ЛЖ, см | 5,54 | 5,15 | 5,76 |
| КСО ЛЖ, мл | 41,9 | 52,9 | 45,1 |
| КДО ЛЖ, мл | 123,2 | 120,6 | 130,7 |
| ФИ, % | 66,0 | 56,1 | 65,5 |
| Нарушение сократимости | Нет | Верхушечный и боковой гипокинез | Верхушечный гипокинез |
Обозначения: КДР – конечный диастолический размер.
С целью оценки перфузии сердца больному была выполнена перфузионная томосцинтиграфия миокарда с 99mТс-тетрофосмином (рис. 4). На рис. 4а представлено изображение перфузии миокарда ЛЖ в виде “бычьего глаза” (т.е. плоскостная карта трехмерного изображения ЛЖ, где в центре располагается его верхушка, а по окружности – базальные отделы). Распределение перфузии картировано цветовым градиентом (переход от белого к черному отражает накопление от максимума к минимуму). На верхушке стрелкой указана степень глубокого снижения перфузии. На рис. 4б – трехмерное изображение перфузии миокарда ЛЖ, стрелкой также указано снижение перфузии на верхушке. На рис. 4в представлена количественная оценка перфузии миокарда ЛЖ по сегментам “бычьего глаза”, стрелкой указаны сегменты со сниженной перфузией. На рис. 4г – изображение в сагиттальном срезе, стрелкой указана та же зона сниженной перфузии на верхушке. Нарушение перфузии избирательно на верхушке является признаком диффузных изменений коронарного русла. Эти данные свидетельствуют об изменениях на уровне мелких сосудов миокарда.
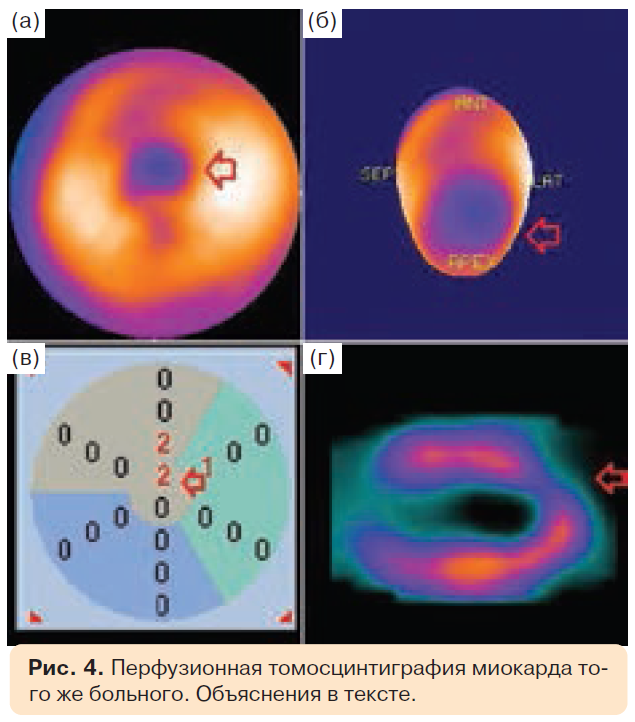
Таким образом, при радионуклидной сцинтиграфии был выявлен достоверный очаг снижения перфузии в верхушечной области, умеренный гипокинез верхушки с переходом на переднеперегородочные отделы ЛЖ, диффузные изменения коронарного русла по типу коронариита и перикоронариита.
Через 2 мес больному О. была продолжена химиотерапия, без антрациклинов, впоследствии проведено облучение остаточных опухолевых масс в средостении, в результате чего достигнута полная ремиссия лимфомы Ходжкина. Пациент до настоящего времени находится под нашим наблюдением, продолжает принимать БАБ и ИАПФ, эпизоды ангинозных болей не повторялись, симптомов сердечной недостаточности не отмечено.
Клинический пример 2. Пациентка З., 32 лет, обследована нами через 10 лет после завершения комбинированного лечения, включавшего химиотерапию и лучевую терапию по поводу диффузной В-крупноклеточной лимфомы с поражением шейно-надключичных, подмышечных, медиастинальных лимфатических узлов, с прорастанием в левое легкое, мягкие ткани передней грудной стенки слева, IVВ стадии. По поводу основного заболевания пациентке было проведено лечение по схеме ACOP (8 курсов), суммарная доза доксорубицина составила 400 мг/м2.
Через 3 года у пациентки развился рецидив заболевания с поражением шейных лимфатических узлов с обеих сторон, была проведена химиотерапия по той же схеме (4 курса ACOP) и лучевая терапия на все лимфатические узлы выше диафрагмы. Суммарная доза доксорубицина, полученная пациенткой за всё время лечения, составила 600 мг/м2. Через 1 мес после окончания лечения больная отметила появление одышки и отеков нижних конечностей.
На протяжении последующих 10 лет пациентка неоднократно обращалась к кардиологу по поводу нарастающей одышки и отеков нижних конечностей, но рекомендуемая терапия ИАПФ, БАБ, диуретиками плохо переносилась и способствовала лишь кратковременному улучшению самочувствия, а симптоматика ХСН непрерывно прогрессировала. Больная поступила в ГКБ № 12 в тяжелом состоянии, с жалобами на одышку при повседневной физической нагрузке (III функциональный класс), выраженные отеки нижних конечностей, сердцебиение, слабость, утомляемость. При аускультации легких выслушивалось значительное количество влажных мелкопузырчатых хрипов на фоне ослабленного дыхания в нижних отделах с обеих сторон, справа дыхание проводилось значительно хуже. Тоны сердца ясные, ритмичные. Артериальное давление 80/60 мм рт. ст., ЧСС 80 в 1 мин. Печень выступает из-под края реберной дуги на 8 см. Массивные отеки нижних конечностей.
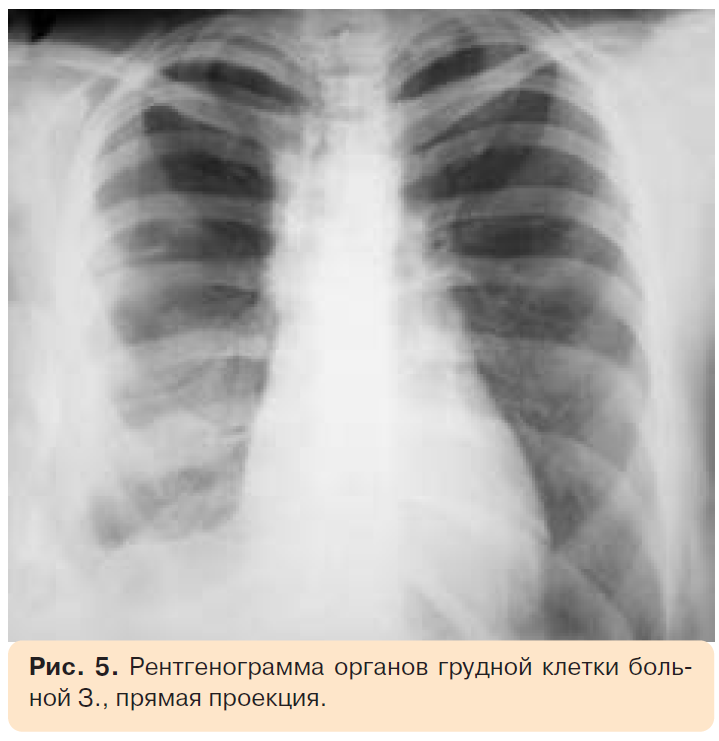
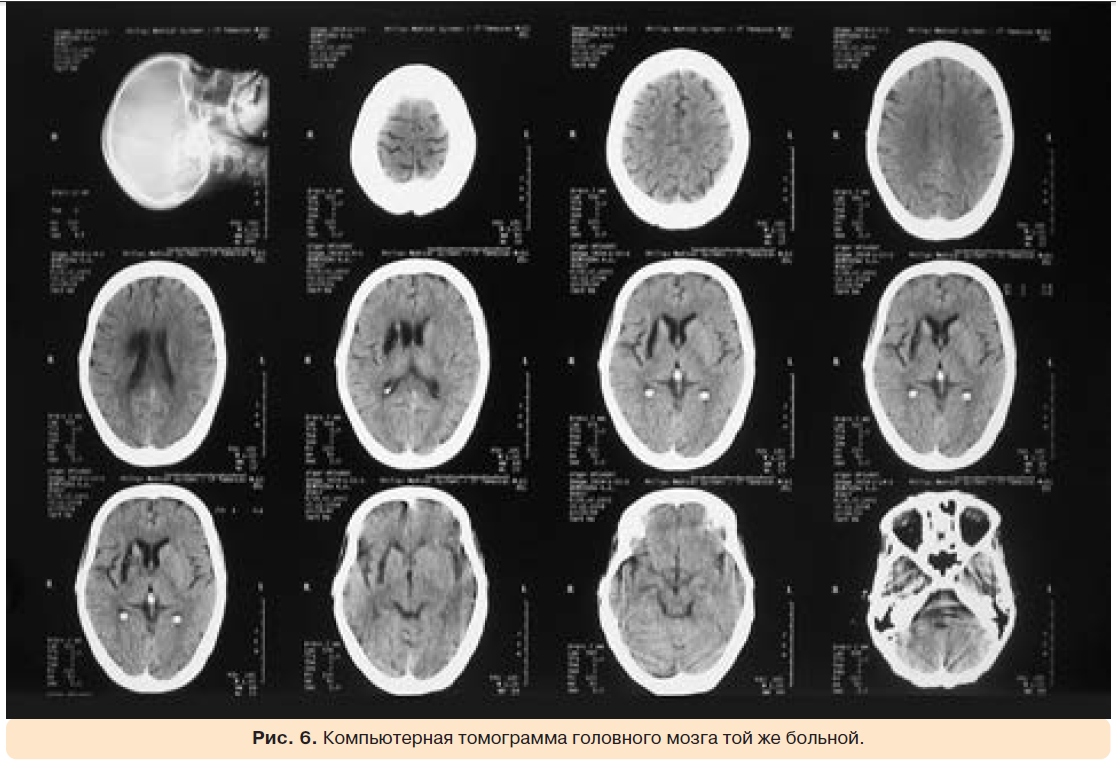
На рентгенограмме органов грудной клетки отмечались признаки застоя в малом круге кровообращения, жидкость в правой плевральной полости, границы сердца не расширены (рис. 5). За несколько месяцев до госпитализации у больной был эпизод дезориентации, сопровождавшийся психотическими нарушениями. В течение нескольких недель симптоматика регрессировала. При компьютерной томографии головного мозга была обнаружена киста в правой гемисфере: в медиальных отделах правой височной области, в проекции скорлупы, определялась зона низкой плотности (1–4 ед. Н) овальной формы, размерами 38×10 мм, с четкими, ровными контурами (рис. 6).
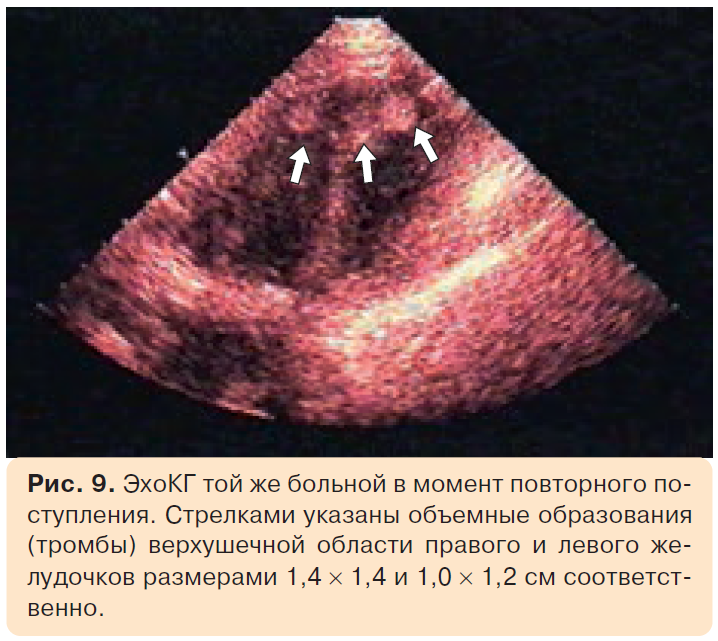
При ЭхоКГ был выявлен выраженный диффузный гипокинез и дискинез верхушечной области, парадоксальное движение межжелудочковой перегородки, выраженное снижение систолической функции ЛЖ (ФИ 25,6%). Резкое снижение систолической функции у больной произошло при отсутствии дилатации ЛЖ, нормальных размерах и объемах полостей сердца (рис. 7, 8). При допплер-ЭхоКГ наблюдалась гемодинамически малозначимая митральная и аортальная регургитация. При динамической ЭхоКГ обнаружен тромбоз желудочков сердца (рис. 9).

В биохимическом анализе крови отмечалось повышение уровня трансаминаз: аланинаминотрансферазы (АЛТ) до 528 ЕД/л, аспартатаминотрансферазы (АСТ) до 520 ЕД/л, гипокалиемия 2,43 ммоль/л. Иммуноферментный анализ на маркеры к гепатиту С был положительным. Учитывая выраженный отечный синдром, больной был назначен лазикс 40 мг утром на фоне внутривенного введения глюкокортикостероидов, верошпирон 150 мг/сут, бисопролол 1,25 мг/сут, дигоксин 0,025 мг 1/4 таблетки/сут, фраксипарин 0,3 подкожно. К регулярно принимаемым диуретикам был добавлен диакарб 500 мг/сут. Постоянная гипотония не позволяла использовать ИАПФ, при попытках их применения артериальное давление снижалось до критического уровня – 50/30 мм рт. ст.
За время лечения в отделении состояние больной заметно улучшилось: отеки нижних конечностей значительно уменьшились, хрипы в легких практически исчезли, оставались лишь единичные сухие хрипы в нижних отделах с обеих сторон, печень сократилась до +2 см от края реберной дуги, уменьшилась слабость. Показатели АЛТ и АСТ снизились до 91 и 65 ЕД/л соответственно, уровень калия достигал 4,34 ммоль/л.
В течение последующих 2,5 лет ХСН оставалась компенсированной на уровне II функционального класса, было отмечено увеличение ФИ ЛЖ с 25,6 до 40,4% и уменьшение КДО со 107,1 до 90,9 мл, улучшение сократимости боковой стенки ЛЖ. Спустя еще 3 года явления ХСН стали вновь постепенно нарастать, участились госпитализации, больная была поставлена в очередь на трансплантацию сердца. При очередной госпитализации больная умерла от прогрессирующей ХСН.
Описанные выше случаи острой и поздней хронической кардиотоксичности протекали с характерными для неклассифицированной кардиомиопатии показателями ЭхоКГ, что наводит на мысль о необходимости расширения протокола обследования пациентов перед проведением химиотерапевтического лечения. Таким больным необходимо проводить динамическое наблюдение между курсами химиотерапии по показаниям и обязательный контроль после окончания всего курса лечения. Следует также рассмотреть необходимость включения в данный протокол помимо ЭКГ и ЭхоКГ коронароангиографии и перфузионной сцинтиграфии миокарда для выявления скрытой коронарной патологии у пациентов с факторами риска сердечнососудистых осложнений. Нужно привлекать терапевтов и кардиологов для совместного с онкологами лечения больных злокачественными заболеваниями и дальнейшего изучения имеющихся проблем.
В настоящее время существует несколько методов, направленных на снижение кардиотоксического действия антрациклинов, таких как:
- соблюдение допустимых доз антрациклиновых антибиотиков;
- изменение общих доз, связанное с факторами риска кардиотоксичности;
- оптимизация режима приема антрациклиновых антибиотиков;
- фармакологическая кардиопротекция;
- использование синтетических аналогов антрациклиновых антибиотиков, характеризующихся более низкой кардиотоксичностью;
- индивидуальная коррекция дозы антрациклинов с учетом данных исследования функции миокарда.
Использование антрациклинов в дозах, не превышающих пороговые, является наиболее частой мерой предупреждения развития кардиотоксичности. Для того чтобы снизить риск сердечно-сосудистых осложнений, были установлены допустимые дозы антрациклиновых антибиотиков, для доксорубицина такая доза составляет 450–550 мг/м2. При увеличении кумулятивных доз риск развития кардиотоксичности резко возрастает, в то же время некоторые пациенты могут переносить кумулятивные дозы, в 2 раза превышающие пороговую, что подчеркивает значимость индивидуальных различий.
Изменения режима дозирования антрациклинов направлены на снижение их максимального уровня в плазме. В исследованиях фармакокинетики выявлено, что высокие разовые дозы чаще вызывают кардиотоксические осложнения, чем длительное применение препарата в более низких дозах. Кроме того, антрациклиновая кардиомиопатия реже встречается у взрослых пациентов, принимавших доксорубицин с интервалами в 1 нед, чем у пациентов, получивших суммарно такую же дозу, только единовременно каждые 3 нед.
Также было показано, что риск поздних сердечно-сосудистых осложнений снижается при увеличении времени инфузии до 48–96 ч. Однако некоторые авторы указывают на спорность терапевтической эффективности и повышенный риск инфекции при увеличении длительности инфузии.
Перспективным направлением является разработка кардиопротективных препаратов. Наиболее эффективная защита кардиомиоцитов при химиотерапии антрациклинами ассоциируется с дексразоксаном (ICRF-187 – кардиоксан). Применение кардиоксана ограничено дозозависимой миелосупрессией (нейтропения III–IV градации) в соотношении с доксорубицином 10 : 1. Профилактическое применение дексразоксана особенно рекомендовано у детей и у больных, входящих в группы риска. В то же время, хотя препарат подтвердил свою эффективность в предотвращении острой антрациклиновой кардиотоксичности, его кардиопротективная роль в отдаленном периоде остается неопределенной.
В современной онкологии ведется разработка новых препаратов группы антрациклинов с высоким терапевтическим эффектом и минимальной кардиотоксичностью. Был создан ряд антрациклинов природного происхождения, полусинтетических и синтетических, а также синтетические препараты групп, близких к антрациклинам, – антрацендионы (митоксантрон, аметантрон, бизантрен) и антрапиразолы (пироксантрон, лозоксантрон). Доклинические и клинические исследования проводились с идарубицином, эпирубицином, зорубицином, алкарубицином, эзорубицином. Кардиологические осложнения были установлены для всех вышеназванных производных. Было обнаружено, что эти препараты при использовании доз с
эквивалентным противоопухолевым эффектом вызывают в кардиомиоцитах повреждающие процессы, похожие на таковые при приеме антрациклинов I поколения.
В последние годы активно изучаются возможности создания липосомных форм антрациклинов. Принцип создания таких препаратов заключается в том, что активный антрациклин включается в состав липидсодержащих микроскопических сфероидов в составе их оболочки или в их содержимом и вводится внутривенно. Эта лекарственная форма, по-видимому, менее токсична при сохранении терапевтической активности.
Тем не менее всё еще не разработаны антрациклиновые препараты с цитостатическим эффектом, сравнимым с эффектом доксорубицина и даунорубицина, которые в то же время не будут иметь кардиотоксической активности.
Необходимо проводить индивидуальную коррекцию химиотерапевтического лечения, основываясь на реакции сердечно-сосудистой системы больного на действие антрациклинов. В связи с этим рекомендуется динамическое наблюдение для оценки функции миокарда, изменения или прекращения химиотерапии при обнаружении ранних нарушений. Разработаны следующие рекомендации для больных, получающих антрациклиновые антибиотики:
- препараты не следует применять у больных с ФИ менее 30%;
- если исходная ФИ составляет 30–50%, функцию ЛЖ нужно оценивать перед каждой новой дозой антрациклинов;
- общим действующим критерием, требующим отмены антрациклиновой терапии, является снижение ФИ ЛЖ более 10% от исходного уровня в течение терапии или на 30% и ниже за время химиотерапевтического лечения;
- если исходная ФИ ≥50%, в дальнейшем ее следует измерять при получении больным суммарной дозы 300–350 мг/м2;
- в соответствии с данными, полученными в нашем исследовании, необходимо также выявлять больных с быстрым снижением КДО (индексированного КДО) после окончания лечения.
Для выявления антрациклинового поражения сердца могут быть использованы циркулирующие в крови маркеры – тропонины. Повышенный уровень тропонинов положительно коррелирует с дозой применяемых антрациклинов. Было выявлено, что уровень тропонина Т был повышен у 30% детей и уровень тропонина I – у 33% взрослых в период от 17 до 72 ч после терапии. Нередко концентрация тропонинов остается повышенной в течение месяцев после окончания терапии. У взрослых пациентов повышенный уровень тропонина I коррелирует с большим снижением ФИ (на 16%), чем у тех, у кого уровень тропонина не повышен (не более 5%).
В настоящее время не существует специфического лечения кардиомиопатии, развивающейся на фоне применения противоопухолевых препаратов. Эффективность дигоксина при этом виде поражения сердца и ХСН чаще всего временная. β-адреноблокаторы (метопролол, лабеталол и др.) с определенным успехом используются для лечения детей с систолической дисфункцией; ИАПФ (эналаприл, каптоприл и др.) могут применяться у больных с повышенной постнагрузкой и бессимптомной систолической дисфункцией ЛЖ.
В соответствии с нашим опытом, у больных с тяжелой застойной сердечной недостаточностью хорошего эффекта можно добиться путем осторожного применения диуретиков. При этом препараты следует принимать ежедневно, дозу нужно титровать до диуреза +200 мл к выпитому количеству жидкости в день. Обязательна диета со значительным снижением количества потребляемой соли (до 1–2 г/сут). Поскольку нередко у таких больных имеет место небольшая полость ЛЖ и низкое артериальное давление, мы несколько недель и даже месяцев не применяем ИАПФ. Благоприятный эффект достигается при применении БАБ, бисопролола в сочетании с дигоксином, в том числе и при синусовом ритме. Доза бисопролола титруется до достижения ЧСС 58–60 в 1 мин. Только при стабильном состоянии и повышении артериального давления до нормы следует попытаться осторожно присоединить ИАПФ, начиная с минимальных доз.
Источник: Шуйкова Ксения Валерьевна, Емелина Елена Ивановна, Гендлин Геннадий Ефимович, Сторожаков Геннадий Иванович Кардиотоксичность современных химиотерапевтических препаратов // Атмосфера. Новости кардиологии. 2012. №3.



